


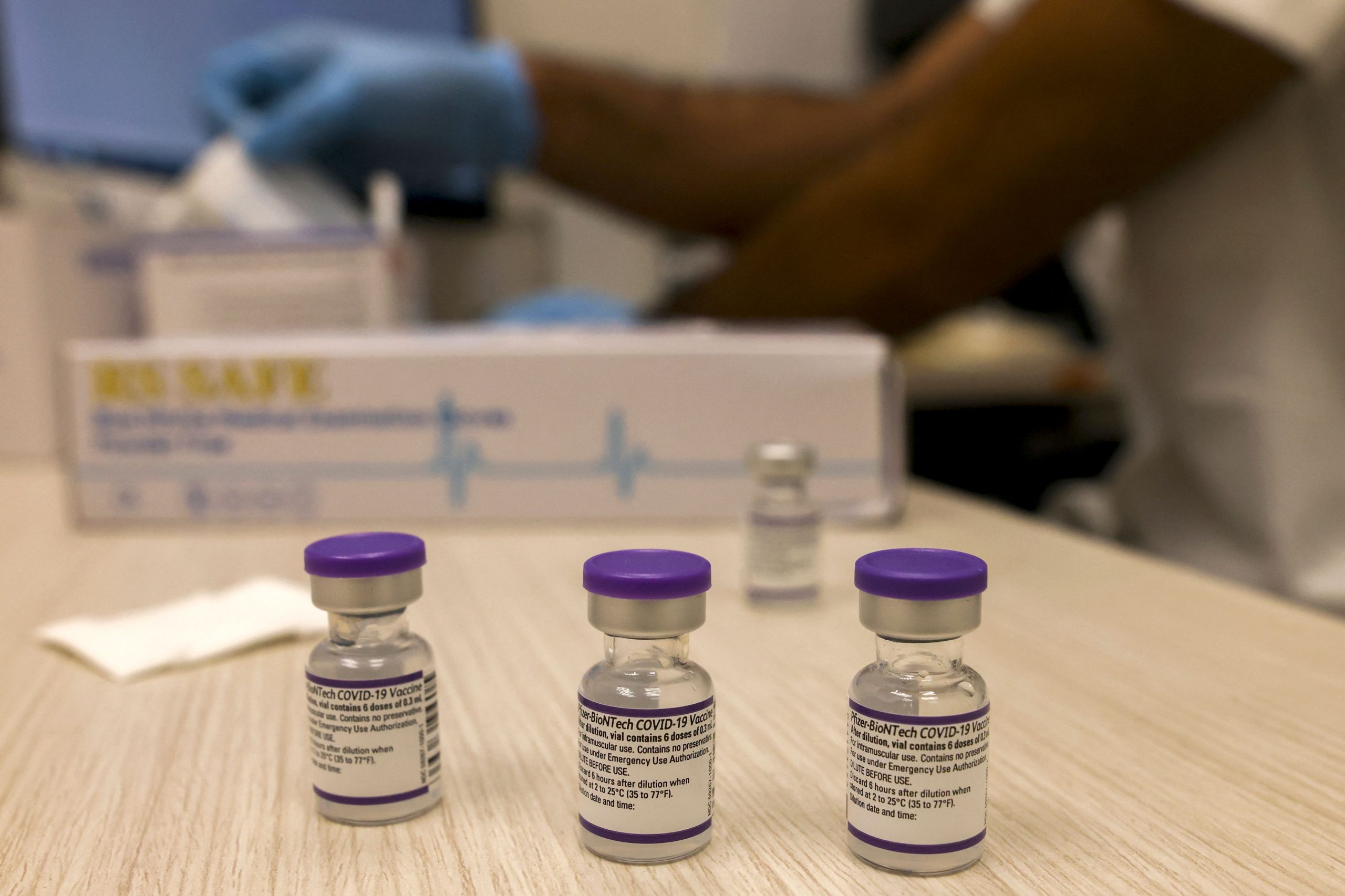
(華盛頓31日綜合電)美國疾病控制預防中心(CDC)的顧問委員會週一一致通過,建議為16歲或以上民眾提供輝瑞BioNTech冠病病毒疫苗。
這是繼美國食品及藥物管理局(FDA)上週全面批准使用輝瑞BioNTech疫苗後,另一個被視為有助推動當局要求民眾接種疫苗的措施。
ADVERTISEMENT
顧問委員會在會上亦有討論為民眾注射冠病疫苗加強劑的建議,決定在下月20日再開會討論,會上亦有成員表示,委員會在討論有關事宜前,白宮已經宣佈下月為民眾注射加強劑,對此表示關注。
全國廣播公司商業頻道(CNBC)報道,近期有跡象顯示輝瑞∕BNT疫苗的保護力在接種一段時間後減弱。輝瑞要求監管機構,容許接種第三劑疫苗作為加強劑。
美國總統拜登上週五表示,監管機構正在考慮在完成免疫接種人們的5個月後,額外施打第三劑疫苗。
輝瑞/BioNTech疫苗是於去年12月通過FDA的緊急授權 (EUA)。據CDC的數據,自去年輝瑞通過EUA以來,全美已施打了超過2.09億劑該疫苗。
CDC數據顯示,目前16歲以上美國人仍有38%未接種,未接種者中有20%認為只有在必要情況下才會接種疫苗。
輝瑞9月公佈試驗數據 5至11歲兒童有望秋季接種
另外,輝瑞董事會成員、美國食品暨藥物管理局(FDA)前局長高特里布表示,針對5至11歲兒童使用的輝瑞BioNTech冠病疫苗,有望在今年秋末或初冬獲得FDA緊急授權使用。
輝瑞下月會公佈5至11歲兒童接種疫苗的臨床數據,稍後提交食品藥物管理局審批,相信審批時間約4至6星期。
ADVERTISEMENT
热门新闻





百格视频





ADVERTISEMENT

































