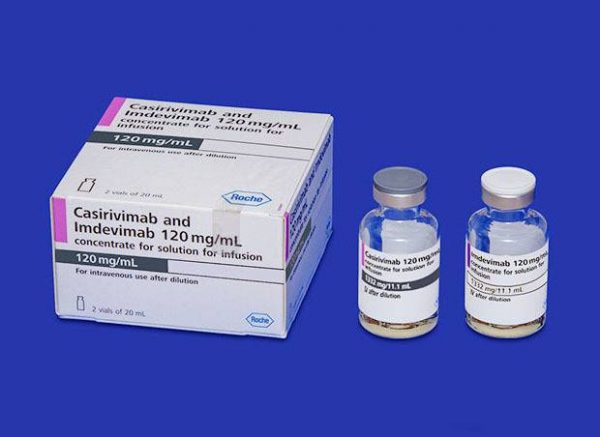
(八打灵再也14日讯)卫生部宣布,有条件批准使用冠病抗体混合药物Ronapreve治疗及预防冠病。
卫生总监丹斯里诺希山今日发文告指出,昨日召开的第367次药品控制执法组(PBKD)会议同意有条件批准含有浓度达120mg/ml的Casirivimab和Imdevimab活性物质的Ronapreve。
ADVERTISEMENT
Ronapreve是的注册持有人是罗氏(大马)私人有限公司(Roche (Malaysia) Sdn. Bhd.),是由瑞士罗氏药厂(F.Hoffman-La Roche Ltd)所生产,使用方式为注射或输液。
药品控制执法组有条件批准Ronapreve适用于以下两种情况:
·治疗:适用于治疗成人和12岁及以上青少年、体重至少40公斤且不需要补氧、有增加的风险发展为严重疾病的冠病患者。
·预防:适用于预防成人和12岁及以上青少年、体重至少40公斤且曾接触或处于接触冠病病毒高风险者,或因身体病况而不太可能对疫苗产生作用或不受冠病疫苗所保障,或未接种冠病疫苗者感染冠病。
诺希山指出,Ronapreve并不是要取代冠病疫苗和公共卫生反应尤其是遵守标准作业程序(SOP)。
他说,卫生部的有条件批准,是需要根据即时的最新数据,以针对该产品的质量、安全及效能资料进行监督和评估,并确保Ronapreve的好处大于风险。
此外,国家药剂监管机构(NPRA)也有批准了默沙东(大马)私人有限公司(Merck Sharp & Dohme (Malaysia) Sdn. Bhd.)和美国Patheon制药公司为预防冠病药物“莫那比拉韦”(Molnupiravir)MK-4482 200mg胶囊所申请的临床试验进口许可证。
“第三阶段的临床试验将在马来西亚的两所研究中心进行,目标是20名18岁及以上的受试者。这项研究预计将历时9个月,是涉及多国的全球研究的一部分。”
Kenyataan Akhbar Kementerian Kesihatan Malaysia
Keputusan Mesyuarat Pihak Berkuasa Kawalan Dadah Kali Ke-367 Berkenaan Pendaftaran Produk Bagi Rawatan dan Pencegahan COVID-19 pic.twitter.com/8GkJ3fYzdm
— KKMalaysia🇲🇾 (@KKMPutrajaya) December 14, 2021



ADVERTISEMENT
热门新闻





百格视频





ADVERTISEMENT

































