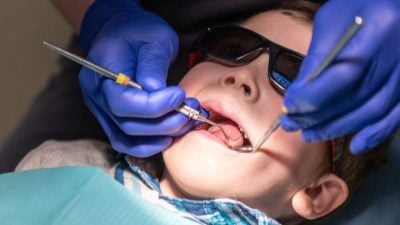
(北京26日综合电)国药集团中国生物的奥密克戎(Omicron)变种株冠病病毒灭活疫,周二获中国国家药监局临床批件。同天,药监局正式批准科兴控股生物技术有限公司基于Omicron研制的冠病病毒灭活疫苗进入临床研究,用以评价新冠病毒变异株疫苗在各类人群中的安全性和免疫原性。
中国生物技术股份有限公司表示,根据国家药监局改良型冠病疫苗指导原则和研发策略,完成工艺验证、质量标准研究、动物体内安全性评价和免疫原性研究,结果显示Omicron冠病灭活疫苗可以针对有关病毒株产生高度中和抗体。
ADVERTISEMENT
中国生物指,北京和武汉生物制品研究所上月与香港研究机构确定临床方案及相关细节,已获得中国药品食品检定研究院的检定合格报告,本月向香港衞生署提交了临床申请资料,并已获得伦理批件和临床研究批件,成为全球最早获批进入临床的Omicron灭活疫苗。
中国生物介绍称,这次获得药监局颁发的临床批件后,公司将采用随机、双盲、队列研究的形式,在已完成2或3剂新冠疫苗接种的18岁及以上人群中进行序贯免疫临床研究,评价Omicron冠病病毒灭活疫苗的安全性和免疫原性。
科兴方面表示,自2021年11月Omicron开始在全球范围内传播后,即迅速采取行动,积极开展Omicron冠病病毒疫苗的研制工作。今年4月14日,科兴基于Omicron变种株研制的冠病病毒灭活疫苗在香港特区获得临床批件。
科兴表示,下一步,将继续与全球合作伙伴持续展开广泛的合作,积极推动在不同人群中接种原型疫苗对冠病病毒变异株的各项研究,以及变种株制备的冠病疫苗进行序贯接种研究,持续为中国和全球冠病疫情防控做出积极贡献。




ADVERTISEMENT
热门新闻





百格视频
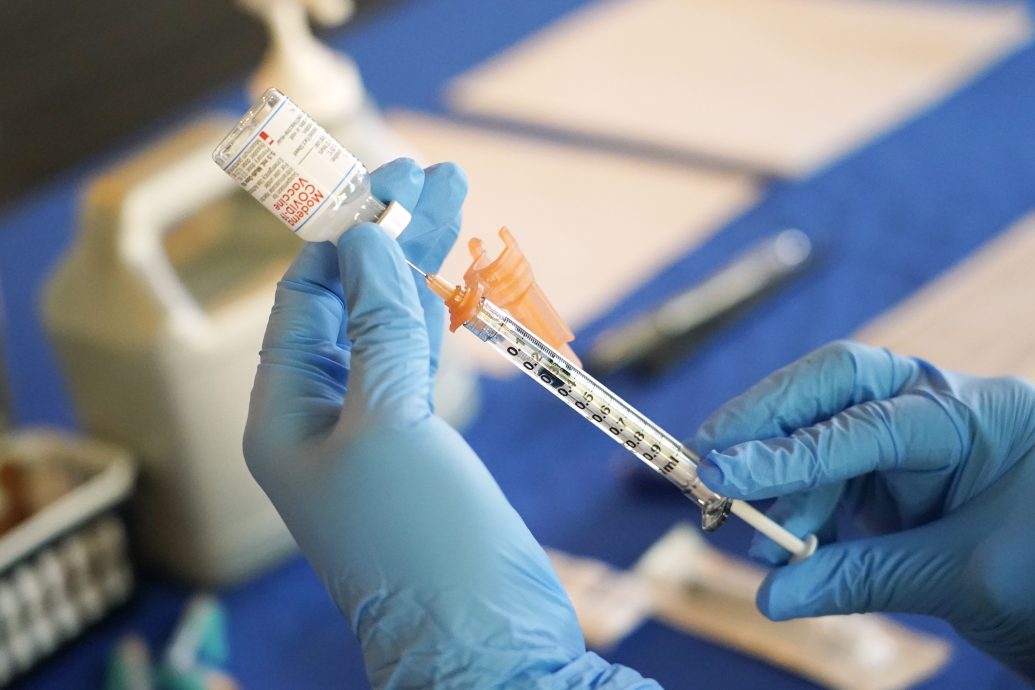
(洛杉矶12日综合电)尽管全球冠病疫情相对而言已经趋缓,且各国早已开放来自国外的观光客,由于冠病病毒持续变种,且眼下即将迎来农历春节,返乡团聚、南来北往,以及各种团体聚会下,恐将迎来疫情的新一波高峰。最新研究显示,如果只有过去旧疫苗的保护力,防护力可能趋近于零!
美媒《洛杉矶时报》报道,虽然全球冠病疫情已经渐缓,可是奥密克戎(Omicron)变异株仍旧持续突变,目前在流行变异株包括XBB.15、XBB.1.16、XBB.2.3.2,其中XBB.1.5.和XBB.1.是奥密克戎的BA.2子变体两个不同版本的组合,皆擅长与ACE2受体(冠病病毒棘蛋白攻击细胞引发感染的部分)结合,是目前最新、最大且最具传染染的最强变种。
南加州大学凯克学院分子微生特和免疫学教授、知名病毒学家坎农惊叹,“这只是最新、最大、传染性最强的变种,令我惊讶的是,这种病毒不断找到新的技俩,使自己更具传染性,甚至更具传播性。”
坎农补充,XBB是目前最具传染性的亚变种,比起其他亚变种更能有效躲避疫苗、先前加强剂接种,或是先前感染时所带来的免疫力,在深秋出现引发新一波疫情后,在节庆期间迅速在室内聚会扩散。
美国的最新研究指出,表示18岁以上成年人要是未接种过XBB疫苗,即使先前曾接种过任何“旧款”冠病疫苗,在这波XBB疫情影响下保护能力也会严重衰退到从未接种过任何冠病疫苗的人相当,包括要是过去接种BA.4/5次世代疫苗,相比从未施打疫苗的族群,在住院方面仅剩22%效益、急诊方面也只剩8%效益。
近日丹麦、荷兰发布的最新研究指出,XBB疫苗可让65岁以上老年族群重症住院风险下降76.1%,且各国研究皆一致指出,接种XBB疫苗的民众能够拥有60至70%的保护力。(ettoday)








ADVERTISEMENT